In questo articolo ti spieghiamo tutto sulla temperatura di fusione e sul punto di fusione di una sostanza.
Ma non solo.
Temperatura e punto di fusione sono infatti due concetti che troppo spesso vengono usati impropriamente ma che, in realtà, solo chi conosce bene sa distinguere.
Alla fine di questo articolo non solo saprai cos’è la temperatura di fusione delle principali sostanze e metalli, ma saprai riconoscere e usare correttamente questi due termini.
La prima cosa che devi sapere è che temperatura di fusione e punto di fusione non sempre sono la stessa cosa.
Temperatura di fusione
La temperatura di fusione di una sostanza è la temperatura alla quale la stessa passa dallo stato solido a quello liquido.
In altre parole, è la temperatura limite alla quale l’energia termica ricevuta dal calore supera l’energia di coesione tra le particelle del reticolo cristallino nella struttura solida, spezzando i legami e consentendo alle particelle atomiche di muoversi abbastanza liberamente da passare allo stato liquido della materia.
Affinché questo accada, la temperatura non aumenta costantemente ma segue 3 curve particolari:
- Curva 1 – Aumento della temperatura
L’energia termica fornita al materiale solido aumenta la sua temperatura in modo costante fino a raggiungere il punto di fusione specifico del materiale.
- Curva 2 – Temperatura costante (Plateau di fusione)
Quando la temperatura raggiunge il punto di fusione, inizia il processo di fusione.
Nonostante l’ulteriore apporto di energia termica, la temperatura rimane costante.
Questo plateau corrisponde al periodo in cui il materiale sta passando dallo stato solido a quello liquido.
L’energia termica viene utilizzata per superare le forze di attrazione intermolecolari senza contribuire ad aumentare ulteriormente la temperatura.
Questa fase è caratterizzata da un cambiamento di stato senza un cambiamento di temperatura.
- Curva 3 – Aumento della temperatura (Dopo la fusione completa)
Una volta completato il processo di fusione, il materiale è diventato liquido e la temperatura inizia nuovamente ad aumentare.
L’energia termica fornita contribuisce all’aumento costante della temperatura del materiale liquido fino a quando non è raggiunta la temperatura desiderata (per eventuali lavorazioni industriali) o fino a quando si innescano altre fasi di cambiamento di stato (evaporazione o ebollizione).
Quasi tutte le sostanze rispettano queste 3 curve, ad eccezione dei solidi amorfi.
Il vetro, per esempio, non ha un punto di fusione definito, ma solo un intervallo di temperatura in cui progressivamente si avvicina al punto di liquefazione.
In casi come questo, si parla di punto di rammollimento.
La curva di fusione
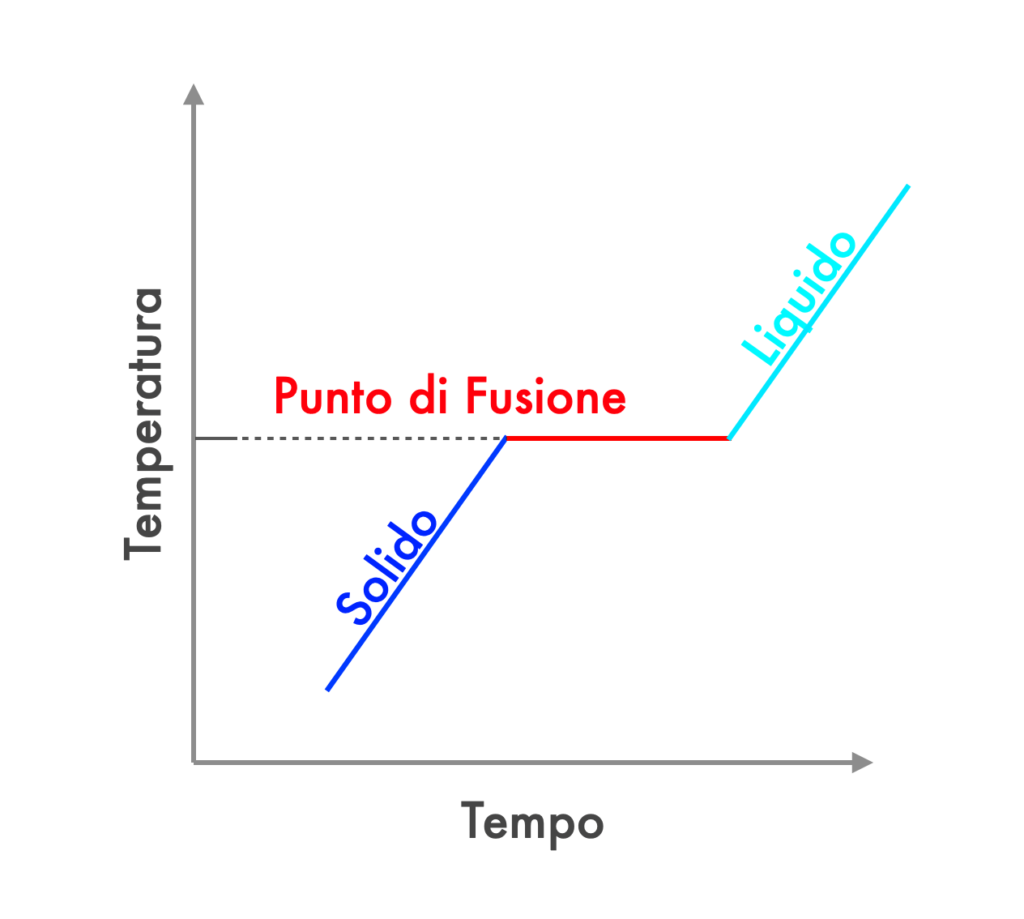
La temperatura di fusione è una proprietà fisica specifica di ciascuna sostanza e può variare notevolmente da una sostanza all’altra.
Ad esempio, l’acqua fonde a 0 gradi Celsius, il tungsteno (un metallo refrattario) fonde alla temperatura altissima di 3422 gradi Celsius mentre l’elio (un gas nobile) all’estremo opposto, -272,2 gradi Celsius.
La temperatura di fusione è influenzata da fattori come la pressione atmosferica e può essere utilizzata come caratteristica distintiva per identificare e classificare le sostanze.
Fino ad adesso, infatti, abbiamo dato per scontato di essere sottoposti alla sola forza della pressione atmosferica di 1 atm (101325 Pa).
Se così non fosse stato, quanto avrebbe influito la pressione sulla temperatura di fusione di una sostanza?
Influenza di pressione e temperatura nel processo di fusione
La temperatura di fusione è una proprietà fisica della maggior parte delle sostanze ed è influenzata dalla pressione.
Per semplificare, possiamo riassumere tutto questo in una regola generale.
In caso di aumento di pressione:
- la temperatura diminuisce in quelle sostanze che si contraggono (diminuiscono il proprio volume) al passaggio dallo stato solido allo stato liquido (es. il ghiaccio)
- la temperatura aumenta in quelle sostanze che si dilatano (aumentano il proprio volume) al passaggio dallo stato solido allo stato liquido (es. i metalli)
Ciò significa che:
- Se P’ > P, V’ < V, un aumento di pressione favorisce la fusione, rendendo necessaria minor energia sotto forma di calore per rompere i legami del reticolo cristallino
- Se P’ > P, V’ > V, un aumento di pressione ostacola la fusione, rendendo necessaria più energia sotto forma di calore per rompere il reticolo cristallino e passare allo stato liquido
Dove:
P’ è l’aumento di pressione
P è la pressione standard
V’ è il volume dopo la fusione
V è il volume prima della fusione
Punto di fusione
Abbiamo dimostrato che:
- La temperatura di fusione è una proprietà fisica specifica di ciascuna sostanza
- La temperatura di fusione è influenzata da fattori come la pressione atmosferica
- Al variare della pressione, varia anche la temperatura di fusione
Come è possibile dunque stabilire una temperatura di fusione standard per ogni sostanza, se è sufficiente che cambi la pressione esterna per far cambiare la temperatura?
Ecco l’importanza del concetto di punto di fusione.
Il punto di fusione si definisce come uno stato termodinamico individuato da tutte le coppie di valori temperatura-pressione alle quali la sostanza passa dallo stato solido allo stato liquido.
In altre parole, il punto di fusione è definito da una certa temperatura (detta temperatura di fusione) e pressione, in corrispondenza del quale si ha il processo di fusione.
- alla pressione costante di 1 atm, punto e temperatura di fusione coincidono
- al variare della pressione, varia anche la temperatura di fusione
Va detto che, nella maggior parte dei casi, si è soliti considerare per convenzione la pressione standard atmosferica, praticamente costante, ed equivalente ad 1 atm (101325 Pa).
Va anche detto che, con pressione diversa dal suo valore standard, è comunque difficile che questa basti per influire significativamente sulla temperatura di fusione, che cambia solo per valori di pressione molto elevati.
Per questi motivi, qualora non specificato, comunemente il punto di fusione viene indicato con la sola temperatura.
Ad esempio, comunemente si dice che il ghiaccio fonde a 0 °C, anche se in teoria sarebbe necessario specificare che questo è vero solo ad una precisa pressione corrispondente con la pressione atmosferica di 1 atm.
Principali sostanze e metalli allo stato puro
Ecco i punti di fusione delle principali sostanze e metalli allo stato puro della tavola periodica degli elementi alla pressione è standard di 1 atm.
| Temperatura di Fusione (°C) | Temperatura di Fusione (K) | Temperatura di Fusione (°F) | |
|---|---|---|---|
| Elio (He) | – 272 | 1 | – 457.6 |
| Idrogeno (H2) | – 259 | 14 | – 434.2 |
| Azoto (N2) | – 210 | 63.15 | – 346 |
| Ossigeno (O2) | – 218 | 55.15 | – 360.4 |
| Cloro (Cl2) | – 101 | 172.15 | – 149.8 |
| Mercurio (Hg) | – 39 | 234.15 | – 38.2 |
| Acqua (H2O) | 0 | 273.15 | – 32 |
| Zolfo (S) | 115 | 388.15 | – 239 |
| Ottone (CuZn) | 1015 | 1288.15 | – 1859.7 |
| Acciaio (Fe, C) | 1370 – 1536 | 1643.15 – 1809.15 | 2497 – 2796.8 |
| Alluminio (Al) | 660 | 933.15 | 1220.3 |
| Argento (Ag) | 961 | 1234 | 1759 |
| Oro (Au) | 1064 | 1337.15 | 1947.9 |
| Rame (Cu) | 1085 | 1358.15 | 1981.3 |
| Ferro (Fe) | 1538 | 1811.15 | 2792.3 |
| Platino (Pt) | 1772 | 2045.15 | 2574.6 |
| Tungsteno (W) | 3422 | 3695.15 | 6211.6 |
Ti lasciamo altri approfondimenti sulla temperatura di fusione di:




